中国科学家团队成功将基因编辑猪肺移植到脑死亡人体内,成为世界首例。8月25日,这项研究被发表在英国学术期刊《自然-医学》上,被誉为异种器官移植领域的“一个里程碑”。
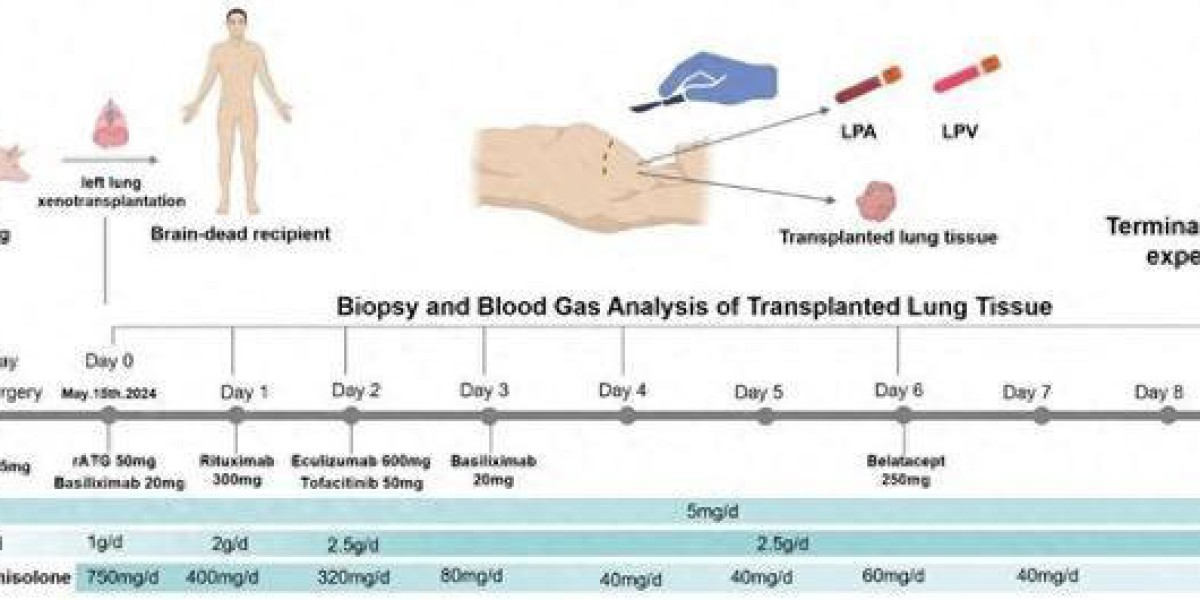
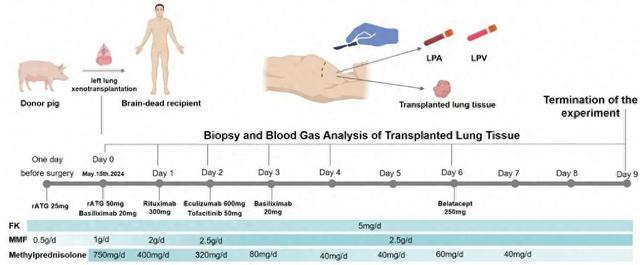
据新华社报道,广州医科大学附属第一医院教授何建行率领的研究团队,将一只经过基因编辑的巴马香猪左肺移植到一名脑死亡者体内,模拟临床常见的单肺移植手术。该供体猪经过6处基因编辑,以降低其器官移植到人体后的免疫风险。
手术后,呼吸、血液、影像等监测数据显示,移植肺维持通气与气体交换功能长达9天,其间未发生超急性排异反应,同步病原学监测也未发现活跃感染迹象。
长期以来,器官短缺是世界性难题。据世界卫生组织统计,全球范围内,每年能得到满足的器官移植需求不到10%。在我国,每年约有30万末期器官功能衰竭患者需要移植,但器官的供需比仅为1:30。
将动物器官移植给人类的异种器官移植是当今全球医学研究的前沿领域,截至目前,全球已完成了数十例猪大器官的人体移植,涉及心脏、肾脏、肝脏、肺四大器官。
“这次手术是对肺这一最难的器官进行了人体初步验证。” 内科学硕士、资深科普博主阿源告诉九派新闻,从这次试验到未来真正被应用于挽救终末期肺病患者的生命,具体时间很难估算,“当前跨物种移植的核心难点仍集中在物种间的差异性上,如何为其构建更稳定、更有效的免疫系统控制方案,是亟待突破的关键。”
对话阿源。
【1】异种移植领域的最难器官
九派新闻:猪肺移植成功并保持呼吸功能9天,为什么其意义如此重大?它突破了哪些前所未有的难关?
阿源:这次手术是对肺这一最难移植的器官进行了人体初步验证。
这是人类第一次把基因编辑后的猪肺移植到人体里,它验证了一个猜想,就是移植之后,体内能够完成气体交换,并且能够度过最危险的超急性排斥的窗口期。
同时,它还系统地记载了9天内的免疫反应过程。首先是24小时内出现了严重的水肿,后面慢慢缓解,第三到第六天,又出现了抗体介导免疫损伤,就整个过程进行了一次记录和探索。而且没有检出猪源性病毒传播信号,相对来说也是一种安全的保证。
九派新闻:肺是异种移植领域“最难的器官”,它难在哪儿?
阿源:肺是人体一个基础的功能器官,主要负责供氧,它通过我们的气道和外界直接相通,我们吸入的空气有很多微生物,我们的气道(尤其上呼吸道)常年也驻扎着很多微生物和污染物,本身很脏,另外,肺的血供很丰富,它的毛细血管网非常庞大,这就导致它很容易发生感染,它的炎症阈值也很低。
而且肺移植后,会出现缺血再灌注,引发原发性移植物功能障碍,也就是说在移植72小时内,它会出现低氧血症,需要支持治疗才能度过炎症反应导致的肺水肿和气体交换功能障碍时期,所以相对来说肺比较复杂。
而且猪和人毕竟是异种移植,会存在一定的物种差异,出现更强的免疫反应。这些原因加起来,导致它是“最难的器官”。
九派新闻:本次使用的供体猪经过了6处基因编辑,其中敲除的3个基因和引入的3个“保护基因”分别起到了什么作用?
阿源:6处基因编辑主要是用来保护猪肺免于被人体攻击的,它敲除的三个基因相当于猪的种族标记,敲除之后,猪肺就没那么容易被人类的免疫器官发现,不容易出现免疫排斥反应。同时,加入人的3个基因会让猪肺戴上人的免疫保护罩,减少被攻击的风险。
九派新闻:为什么选择脑死亡患者而不是活体患者进行试验?其中的医学和伦理考量是什么?
阿源:选择脑死亡的病人,是因为这次试验的目的是验证而非治疗,验证意味着它本身存在巨大风险,很有可能受体本身无法获益,所以不太可能用活体。尤其是像肺移植这样高难度的手术,对于受体患者来说,是一个非常不负责任的做法。
脑死亡从医学上来说本身属于死亡个体,我们可以通过ECMO等手段让器官保持一定的活性,在伦理审批通过、家属同意、监管机构监管的情况下,在有限时间内观察器官功能,获取相应的数据。另外,对于脑死亡患者,我们可以取样的频次更高一些,更适合用来观察试验。
九派新闻:手术中保留了患者自己的右肺,这是出于什么考虑?
阿源:脑死亡患者需要我们通过一些生命维持设备来维持生命体征,保留右肺可以在进行左肺移植手术的时候给身体提供足够的通气和氧合。同时,放置猪肺后,右肺可以作为对照组来区分,到底是全身因素还是移植物的特异排异反应,这样既保证研究安全,也保证受体基本生命体征的稳定性。
研究团队提供的论文中的示意图。 图/新华社
【2】猪的器官能较好匹配人类移植需求
九派新闻:能否通俗地解释一下什么是“异种移植”?与我们常听说的“捐肾救亲”这类同种移植相比,区别是什么?
阿源:最大的区别就是物种的区别,这一区别导致免疫系统会出现更强大的排异反应。其次,不同物种之间还会存在其他病原体传播,我们要防止因异种移植出现跨物种传染病,所以相对来说它更加复杂。
为了解决这个区别造成的问题,首先,我们要进行基因编辑,把供体动物的器官做到跟人体更加接近。第二,要进行更强的免疫管理,术后观察以及服用的药物会比人与人之间的移植更加复杂。第三,异种移植对于医院和患者也有要求,需要医院能够长期随访和观察患者,尤其是在这个技术才开始实行的时候,确保不会出现感染,不会造成新疾病的传播,确保移植器官不会在体内出现其他反应。
九派新闻:长期以来“免疫排斥”是异种移植的“头号敌人”,就像人体的免疫系统会“攻击”外来的猪器官,目前,在临床试验中这种排斥分哪几种?现在针对不同的排斥,又有哪些“应对办法”?
阿源:器官移植过程中需重点应对三类排斥反应。第一是“超急性排斥”,其发作极具危险性且速度极快,通常在器官接入人体血管后的几分钟至几小时内出现。这是因为人体血液中天然存在的抗体,会迅速识别移植器官为“外来物体”并发起攻击,导致器官即刻失效,进而危及患者生命。针对此类排斥反应,若为同种异体移植(人与人之间),需提前进行供受者配型;若为异种移植(如猪到人),则可通过基因编辑技术规避。
二是“急性排斥”,一般发生在移植后的几天至几周内,主要由两类机制引发:一类是T细胞、NK细胞等免疫细胞渗透至移植器官组织内发起攻击;另一类是B细胞产生的抗体,识别器官中的异种抗原后攻击器官及血管,二者均可能导致器官功能衰竭。为了应对这种情况,就需要在医院内部对患者进行长期观察,并让患者服用一定的免疫抑制剂,以降低自身免疫反应;另一方面,患者需入住特殊病房,避免因服用免疫抑制剂导致免疫力大幅下降时,受到外界病原体侵袭。
三是“慢性排斥”,通常在移植几年后逐渐显现,会慢慢地破坏器官结构、导致功能逐渐丧失。应对此类反应需建立长期随访机制:移植患者需定期到医院复查,通过影像学检查或组织活检,判断器官是否存在炎症反应及功能受损情况;医生则根据检查结果,调整免疫抑制治疗方案,或通过其他药物调节器官功能,以延缓器官衰竭进程。
九派新闻:异种器官移植为什么会选择猪?在异种器官移植发展过程中,学界尝试过哪些物种?
阿源:学界曾于20世纪中期尝试以狒狒、黑猩猩等灵长类动物作为供体来源。从直观认知来看,它们与人类的接近度更高,器官结构的相似性也更高,但实践中却因多重关键问题逐渐被放弃:其一,即便亲缘关系接近,灵长类与人类仍属于跨物种范畴,器官移植后会引发强烈的免疫排斥反应;其二,灵长类与人类过于接近,使得将其作为器官供体时,疾病传播风险突出,灵长类身上携带的病原体更易传染给人类,会增加术前病原体筛查的难度,也提升了术后感染的风险。
相比之下,猪与人类器官适配性高,它的体型与人类接近,能较好匹配人类的移植需求。而且猪的繁殖周期短,不需要很长时间去制造供体。另外,猪的基因组编辑技术相对成熟,相较于灵长类的基因编辑易出现脱靶、人类基因植入难度大等问题,猪的基因更易通过技术手段进行修饰。
九派新闻:用来进行器官移植的猪有哪些特别之处?在这个过程中如何避免跨物种的传染病传播风险?
阿源:作为器官供体的猪会经过专门培育,它的生长环境与普通猪存在本质差异,需要处于完全无菌状态,以杜绝外来菌种、病毒的引入。因此,对其呼吸的空气、饮用的水源、饲料等均需严格把控。
除了饲养条件,供体猪在用于临床之前,还需要经过器官的多轮筛选。并且需对受体进行长期监测,若发现异常情况或潜在传染病风险,需及时处置并纳入公共卫生管理范畴。
广西河池市巴马县“巴马香猪原产地保护基地”养殖的巴马香猪。 图/新华社
【3】物种间的差异性仍是当前异种移植核心难点
九派新闻:异种器官移植应用在病人身上需要满足哪些条件?
阿源:首先需以充足科学数据为支撑:按此前提及的逐步试验、逐步扩大范围、逐步积累观察数据,待数据完善后提交至审批部门,由国家监管机构审核批准,再进入人体临床试验阶段。此阶段可通过同情用药、小范围试点等方式进行初步探索。
同时,技术应用还需满足多方面要求:供体猪需在专门饲养场进行严格饲养,且其遗传结构需保持稳定,避免因繁殖过程中基因变异导致后续批次不合格;开展相关临床操作的医院须具备足够管理能力,不可随意开放资质,以防出现患者与医院管理脱钩的问题。
九派新闻:从这次成功的9天试验,到未来真正应用于挽救终末期肺病患者的生命,除了排斥和病毒,这中间还有多长的路要走?最大的“拦路虎”是什么?
阿源:这个具体时间可能很难估算,因为科学本身就存在很大的不确定性,比如针对长期排斥反应的免疫控制方法何时能研发成功,如何降低免疫抑制剂引发的感染风险等等,未来是否会有更优解决方案,仍需进一步探索;但是当前的探索方向是正确的,比如在动物体内培育器官、单独培育或克隆器官等,我认为当前的跨物种移植的核心难点,仍集中在物种间的差异性上,如何为其构建更稳定、更有效的免疫系统控制方案,是亟待突破的关键。
九派新闻:设想一下,如果未来猪肺移植技术完全成熟,它最先会应用于哪些疾病的治疗?
阿源:猪肺移植与人类肺移植的适用场景基本一致,主要针对经其他治疗手段难以奏效的终末期肺病,具体包括不可逆呼吸衰竭、进展期间质性肺病、特发性肺纤维化、极重度慢性阻塞性肺疾病(COPD)、囊性纤维化、肺动脉高压等。通过跨物种移植,可在一定程度上解决终末期肺病患者因无法等待人类供体而失去生命的困境。
九派新闻记者 李恺 彭茸雯
编辑 李杨
【来源:九派新闻】
声明:此文版权归原作者所有,若有来源错误或者侵犯您的合法权益,您可通过邮箱与我们取得联系,我们将及时进行处理。邮箱地址:jpbl@jp.jiupainews.com
【来源:九派新闻】