《美国心脏协会杂志》,草绿色链球菌生物膜逃避免疫检测并导致动脉粥样硬化斑块的炎症和破裂
牙龈出血和心脏猝死之间可能存在比医学界此前认识到的更为直接和危险的联系。芬兰坦佩雷大学发表的突破性研究首次提供了确凿证据,证明口腔细菌不仅与心血管疾病相关,更是直接参与引发致命心脏病发作的"罪魁祸首"。通过分析217名冠状动脉疾病患者的动脉斑块样本,研究人员发现超过40%的冠状动脉斑块内存在口腔细菌的DNA,这些"入侵者"正在心脏最关键的血管内形成生物膜,为心肌梗死埋下定时炸弹。
隐藏在动脉斑块深处的细菌军团
这项发表在《美国心脏协会杂志》上的研究采用了前所未有的精确检测方法,对121名心脏性猝死患者和96名接受血管手术患者的冠状动脉斑块进行了深度分析。研究团队运用定量聚合酶链反应、免疫组织化学以及转录组学等多种先进技术,成功识别并定位了潜伏在动脉壁内的细菌群落。
研究结果令人震惊:在猝死患者中,42.1%的冠状动脉斑块检测到口腔链球菌的存在,而在手术患者中这一比例为42.9%。这些细菌主要属于变异链球菌群,通常是导致蛀牙和牙龈疾病的常见病原体。更为关键的是,这些细菌并非偶然出现在血管中,而是在动脉粥样硬化斑块的核心区域建立了稳定的生物膜结构。
坦佩雷医生Pekka Karhunen强调了这一发现的重要性:"长期以来,人们一直怀疑细菌参与冠状动脉疾病,但一直缺乏直接和令人信服的证据。我们的研究表明,动脉粥样硬化斑块内确实存在来自几种口腔细菌的遗传物质。"
从口腔到心脏的致命旅程
传统医学观点认为,动脉粥样硬化主要由胆固醇、脂肪和钙质沉积造成,细菌感染只是次要因素。然而,这项研究揭示了一个更加复杂和危险的病理机制:口腔细菌通过血液循环系统迁移到冠状动脉,在动脉壁的脂质核心内建立防御堡垒。
这些细菌生物膜的位置选择极其"狡猾"——它们隐藏在斑块最深处,远离人体免疫系统的监控范围。在这个相对安全的环境中,细菌可以长期潜伏,形成所谓的"休眠生物膜"。这种状态下的细菌代谢活动缓慢,对抗生素治疗具有很强的抗性,但一旦被激活,就可能引发灾难性后果。
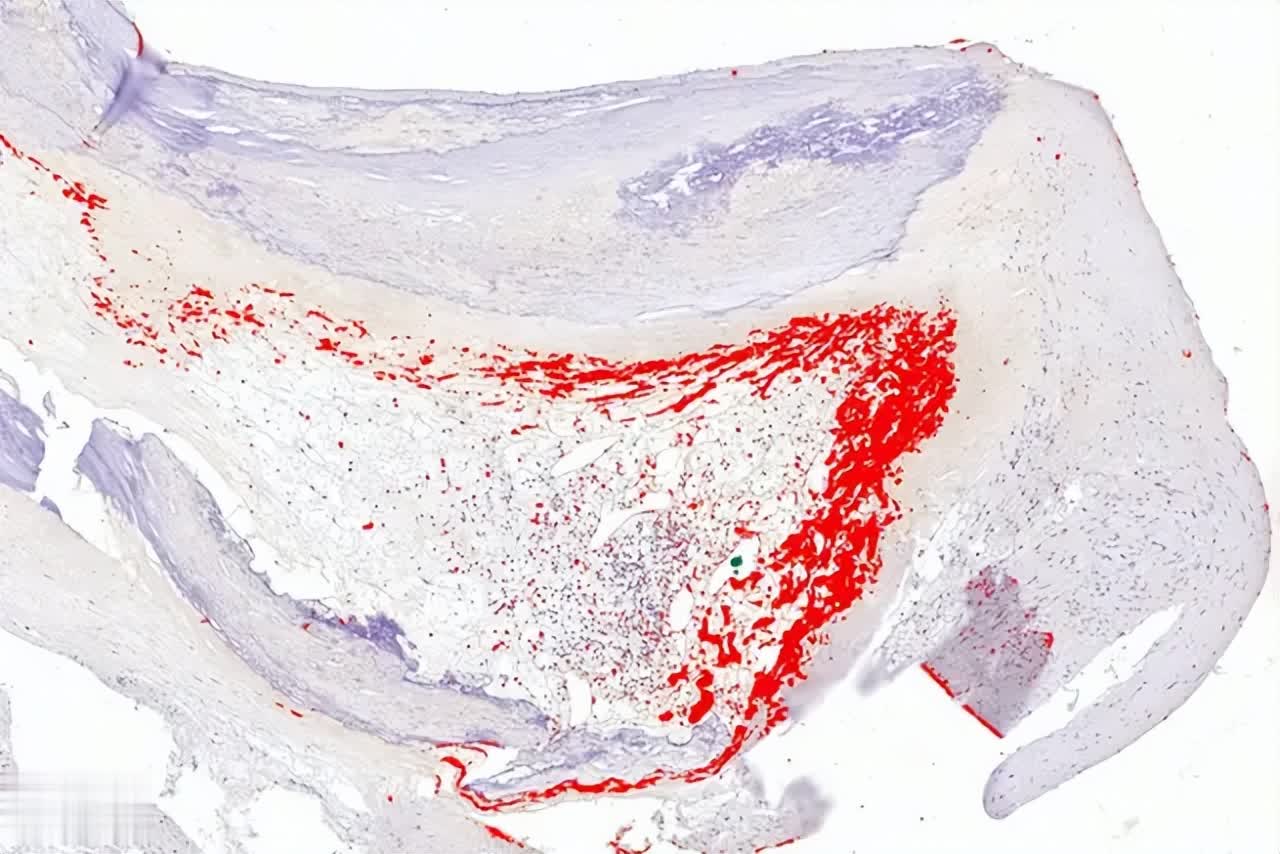
在冠状动脉斑块内发现的细菌生物膜(红色)。当患者遭遇其他应激因素时,如细菌感染、病毒性疾病、不良饮食或心理压力导致的去甲肾上腺素水平升高,休眠的细菌生物膜可能被激活,引发急性炎症反应,最终导致斑块破裂和心脏病发作。
重新定义心血管疾病的预防策略
这一发现对心血管疾病的预防和治疗策略产生了深远影响。传统的心脏病预防主要关注血脂管理、血压控制和生活方式改善,而口腔健康往往被视为相对独立的健康领域。然而,新研究表明,口腔卫生可能是心血管健康管理中被严重低估的关键环节。
过去几十年的流行病学研究已经观察到口腔健康与心血管疾病之间的统计学关联,但一直缺乏明确的因果关系证据。一些大型前瞻性研究显示,患有牙周病的人群心脏病发作风险增加25-50%,而定期进行口腔清洁的人群心血管事件发生率显著降低。
现在,芬兰研究团队的发现为这些统计学关联提供了有力的生物学解释。口腔细菌不再是心血管疾病的"旁观者",而是直接参与疾病进程的"参与者"。这意味着口腔健康管理应该被纳入心血管疾病的一级预防策略中。
临床实践的革命性变化
这项研究的临床意义不仅限于预防层面,还可能改变现有的诊断和治疗方法。研究人员指出,检测冠状动脉斑块中的细菌生物膜可能成为评估心脏病发作风险的新型生物标志物。通过识别携带细菌的不稳定斑块,医生可以更准确地预测哪些患者面临更高的急性心血管事件风险。
在治疗方面,这一发现也开辟了新的可能性。传统的抗生素治疗对于深埋在生物膜中的细菌效果有限,但针对性的抗生物膜治疗策略可能提供新的解决方案。此外,结合口腔治疗和心血管治疗的综合方法可能成为未来医疗实践的新趋势。
研究还提示了一些潜在的干预时机。由于细菌生物膜的激活需要特定的触发因素,识别和控制这些触发因素可能有助于预防急性事件的发生。例如,在感染期间或高应激状态下加强监护,可能有助于降低心脏病发作的风险。
未来研究的方向与挑战
尽管这项研究提供了重要的突破性证据,但仍有许多问题需要进一步探索。首先,口腔细菌是如何准确迁移到冠状动脉并选择性地在特定部位定植的机制仍不清楚。其次,不同类型的口腔细菌是否具有不同的致病性,以及它们之间是否存在协同作用,都需要深入研究。
另一个重要问题是如何开发有效的治疗策略。传统抗生素对生物膜的渗透能力有限,而机械清除又面临技术挑战。研究人员需要探索新的抗生物膜药物或联合治疗方案。
此外,个体差异也是一个重要考虑因素。为什么有些人的口腔细菌会迁移到心血管系统,而另一些人则不会?这可能涉及遗传因素、免疫状态、口腔微生物群落结构等多个方面。
研究团队在论文中总结道:"这一发现为心肌梗死的发病机制增加了新的概念,并为动脉粥样硬化致命并发症的诊断和预防开辟了新的可能性。"这项研究不仅改变了我们对心血管疾病的理解,更重要的是为数百万心脏病患者提供了新的希望和治疗方向。随着后续研究的深入,基于细菌-心血管疾病关系的精准医疗时代可能即将到来。