犹他大学医学院的研究团队在肠道微生物与代谢健康的关系研究中取得突破性进展。他们发现一种名为松孢杆菌的肠道细菌能够通过产生特殊脂质分子,显著降低高脂饮食小鼠的肥胖风险并改善代谢指标。这项发表在《细胞代谢》杂志上的研究不仅确定了这种细菌的保护作用,更重要的是阐明了其背后的分子机制 —— 细菌产生的脂质能够抑制宿主体内有害神经酰胺的积累,从而打破高脂饮食导致肥胖的恶性循环。
全球肥胖危机正在加剧。世界卫生组织数据显示,全球约八分之一的人口患有肥胖症,这一比例在过去几十年中持续上升。肥胖不仅影响生活质量,更是 2 型糖尿病、心血管疾病、某些癌症和多种代谢疾病的重要风险因素。尽管市场上充斥着各种减肥方案,从流行饮食法到高强度运动计划,但长期有效的体重管理仍然是医学和公共卫生领域的重大挑战。近年来,科学家们越来越关注肠道微生物群在代谢健康中的作用,试图从人体内数万亿微生物构成的复杂生态系统中寻找解决方案。
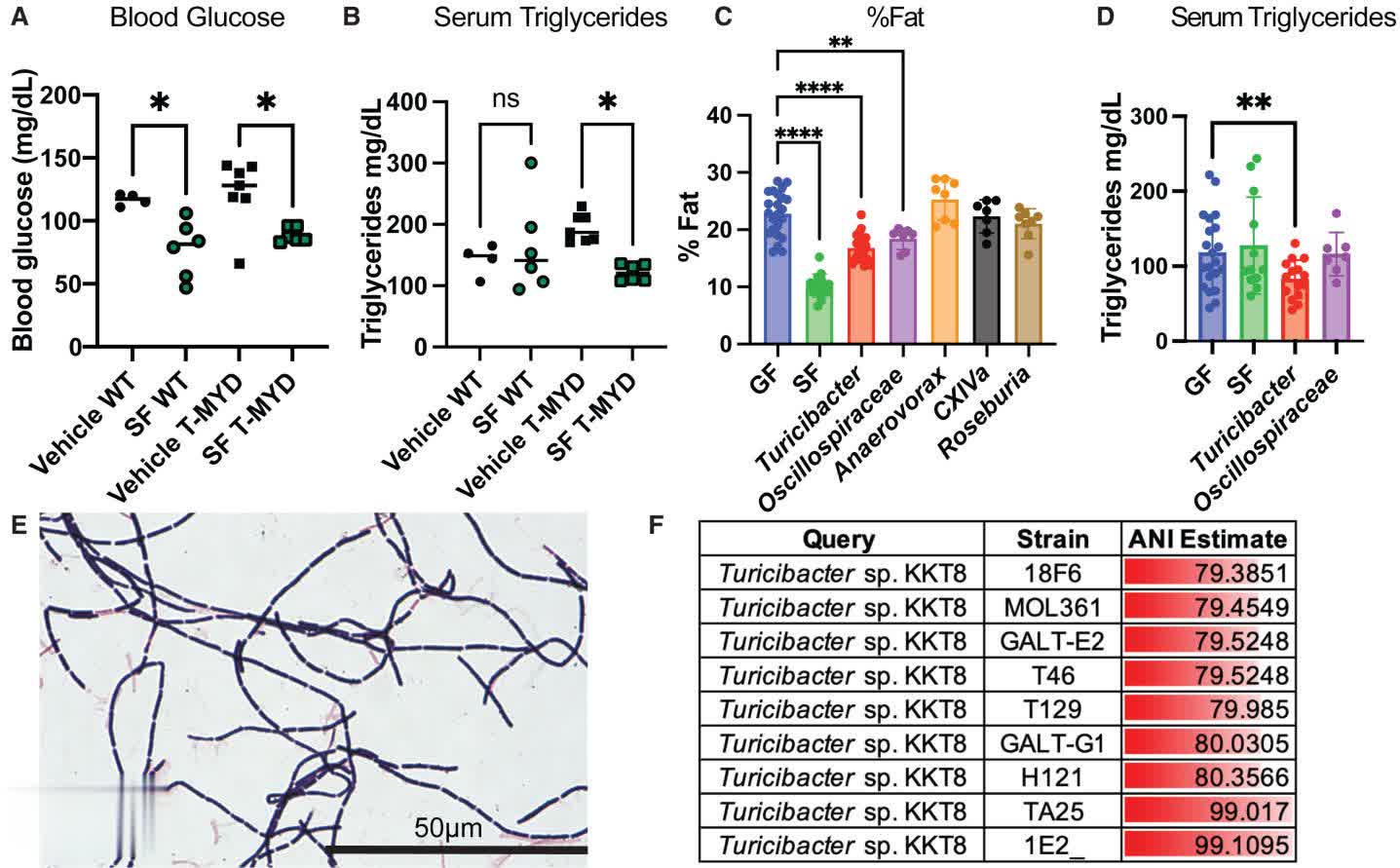
鉴定来自SF群落的瘦身诱导微生物(A和B)(A)8周龄雄性WT和T-MyD88小鼠的空腹血糖和(B)血清甘油三酯在补充SF的HFD上2个月(WT,n = 10;T-Myd88,n = 13)。图片来源:细胞代谢 (2025)。
从关联到因果的科学突破
肠道微生物群与肥胖之间的关联已经被观察多年。早期研究发现,肥胖个体和正常体重个体的肠道菌群组成存在显著差异,某些细菌的丰度与体重指数、脂肪含量等代谢指标呈现相关性。粪便移植实验也表明,将肥胖小鼠的肠道菌群移植给无菌小鼠,可以使后者出现代谢异常。但这些研究面临一个共同的局限:难以从数千种肠道微生物中精确识别出真正起作用的菌株,更难以解释其作用机制。
犹他大学医学院的肯德拉・克拉格及其团队采用了更加精准的研究策略。他们首先从复杂的肠道菌群中分离出松孢杆菌属的特定菌株,这一属的细菌此前已被怀疑与脂肪代谢有关,但缺乏直接证据。研究团队设计了多组对照实验,使用无菌小鼠和标准实验小鼠两种模型,分别喂养常规饮食或高脂饮食,部分小鼠额外补充纯化的松孢杆菌。这种严格的实验设计能够排除其他肠道菌群的干扰,直接评估松孢杆菌的效果。
实验结果超出预期。即使在高脂饮食条件下,补充松孢杆菌的小鼠体重增加明显少于对照组,体脂含量显著降低。更重要的是,这些小鼠的代谢指标全面改善:空腹血糖水平下降,血清甘油三酯浓度降低,胰岛素敏感性提高。这些数据表明松孢杆菌不仅能够预防肥胖,还能改善与肥胖相关的代谢紊乱。有趣的是,这种保护效应在无菌小鼠中更加明显,说明松孢杆菌的作用是直接的,不需要其他肠道微生物的协同。
细菌脂质的意外发现
确认松孢杆菌的保护作用只是第一步,更关键的问题是:这种细菌如何发挥作用?研究团队开始深入分析补充松孢杆菌后小鼠体内的分子变化。他们对肠道内容物和血液样本进行了系统的脂质组学分析,结果发现了一个出人意料的现象 —— 松孢杆菌本身能够产生一类特殊的脂质分子。
这一发现具有重要意义。大多数关于肠道细菌影响宿主代谢的研究都聚焦于细菌代谢短链脂肪酸、胆汁酸或氨基酸等小分子代谢产物,很少关注细菌自身产生的脂质。细菌膜脂质通常被认为主要用于维持细菌自身的结构完整性,与宿主代谢的直接互动关系研究较少。但克拉格团队的数据显示,松孢杆菌产生的脂质不仅存在于细菌细胞中,还能被释放到肠道环境,进而影响宿主的脂质代谢网络。
为了验证这些细菌脂质是否真的是保护效应的关键,研究团队进行了一项巧妙的实验:他们从松孢杆菌培养物中纯化出这些脂质分子,去除所有活菌,然后将纯化的脂质单独喂给高脂饮食的小鼠。令人惊讶的是,即使没有活细菌,这些纯化的细菌脂质也足以预防肥胖和改善代谢指标。这个实验提供了直接的因果证据:松孢杆菌的保护作用至少部分是通过其产生的脂质分子实现的。
神经酰胺通路的新认识
进一步的机制研究揭示了这些细菌脂质如何影响宿主代谢。研究团队发现,松孢杆菌产生的脂质能够抑制宿主体内神经酰胺的生物合成。神经酰胺是一类重要的生物活性脂质,在正常生理条件下参与细胞信号传导和膜结构维持,但在高脂饮食或肥胖状态下会过度积累,导致胰岛素抵抗、炎症反应和脂质代谢紊乱。
高脂饮食引发的神经酰胺积累是代谢疾病的重要病理机制。当摄入过多饱和脂肪酸时,细胞内神经酰胺合成通路被激活,生成的神经酰胺会干扰胰岛素信号传导,抑制葡萄糖摄取,促进脂肪在肝脏和肌肉等组织中异位沉积。许多治疗代谢疾病的药物研发都将降低神经酰胺水平作为目标。松孢杆菌脂质能够天然地抑制神经酰胺合成,为这一研究方向提供了新的思路。
具体的分子机制涉及细菌脂质与宿主细胞膜的相互作用。研究团队的数据表明,松孢杆菌脂质可能通过整合到宿主肠道上皮细胞的细胞膜中,改变膜的脂质组成和物理性质,进而影响膜上神经酰胺合成酶的活性。此外,这些细菌脂质还可能作为信号分子,通过特定的受体激活下游信号通路,调控脂质代谢相关基因的表达。研究团队在论文中写道:“我们的数据识别出一种新型细菌 - 宿主脂质网络,促进宿主代谢健康并具有治疗潜力。”
免疫系统的双重角色
研究还揭示了免疫系统在松孢杆菌保护效应中的作用。团队使用了缺失髓样分化因子 88 基因的小鼠,这种小鼠的先天免疫信号通路受损。结果发现,在这些免疫缺陷小鼠中,松孢杆菌的保护作用反而增强了。这一看似矛盾的发现提示,完整的免疫应答可能部分限制了细菌脂质的效果,或者免疫激活本身就伴随着某些促进肥胖的代谢改变。
这一发现与近年来关于代谢炎症的研究相呼应。慢性低度炎症被认为是肥胖和代谢综合征的重要特征,免疫细胞浸润到脂肪组织并释放促炎细胞因子,加剧胰岛素抵抗和脂质代谢紊乱。松孢杆菌脂质可能不仅通过直接调控脂质代谢发挥作用,还可能通过调节免疫反应间接改善代谢健康。在免疫功能受损的小鼠中,这种炎症负担减轻,细菌脂质的直接代谢效应得以更充分地展现。
人类应用的前景与挑战
动物实验的成功自然引发了人类应用的问题。研究团队对人类样本进行了初步分析,发现肥胖个体肠道中松孢杆菌的丰度确实显著低于正常体重个体。这一关联性支持了动物实验结果的临床相关性,提示松孢杆菌可能在人类代谢健康中也扮演重要角色。如果能够开发出含有松孢杆菌或其脂质产物的益生菌补充剂,可能为肥胖和代谢疾病提供新的预防和治疗手段。
然而从实验室发现到临床应用还有很长的路要走。首先需要解决的是菌株选择和培养问题。松孢杆菌属包含多个种和亚种,不同菌株的脂质产生能力和代谢效应可能存在差异。研究团队使用的特定菌株能否在人类肠道中稳定定植和发挥作用,需要临床试验来验证。其次,细菌脂质的结构复杂,精确鉴定其有效成分并实现规模化生产具有技术挑战。如果选择直接补充纯化脂质而非活菌,还需要解决脂质的稳定性、生物利用度和给药方式等问题。
安全性评估也至关重要。虽然松孢杆菌是人类肠道的天然成员,一般被认为是安全的,但长期大剂量补充可能带来未知风险。肠道微生物生态系统极其复杂,引入或增加某一种细菌可能对其他菌群产生连锁影响。此外,个体间肠道菌群差异很大,同一种益生菌干预在不同人群中的效果可能不同,甚至在某些情况下可能无效或产生负面作用。这些问题都需要通过严格的临床前研究和临床试验来回答。
微生物代谢组学的新时代
这项研究的更广泛意义在于,它为微生物组研究提供了新的范式。过去十年间,大量研究描绘了肠道菌群与各种疾病的关联图谱,但从关联到机制,从机制到应用的转化一直进展缓慢。主要障碍在于肠道菌群的复杂性 —— 数千种微生物相互作用,产生数万种代谢产物,形成错综复杂的生化网络。试图从这个黑箱中找出具体的有效成分和作用机制,如同大海捞针。
克拉格团队的研究展示了一种有效的策略:首先通过严格的分离和纯化确定特定菌株的因果作用,然后系统地分析该菌株产生的代谢产物,筛选出关键的效应分子,最后阐明这些分子影响宿主的具体机制。这种从菌株到分子,从分子到机制的逐层深入方法,可以应用于其他微生物 - 宿主互作的研究。随着代谢组学、蛋白组学和基因编辑等技术的进步,这种精准的机制研究将变得更加可行。
细菌脂质作为微生物 - 宿主互作的媒介,是一个相对新颖但潜力巨大的研究方向。除了松孢杆菌,其他肠道细菌也可能产生具有生物活性的脂质分子。不同细菌产生的脂质在结构和功能上可能存在差异,有些可能促进健康,有些可能致病。系统地表征肠道菌群的脂质多样性,阐明不同细菌脂质对宿主代谢、免疫和神经系统的影响,将是未来微生物组研究的重要方向。
个性化微生物疗法的愿景
从更长远的视角看,这项研究推动了个性化微生物疗法的发展。传统的饮食和运动干预对肥胖的效果因人而异,部分原因可能在于个体间肠道菌群的差异。如果能够通过检测个体的肠道菌群组成,识别出缺乏有益菌或富集有害菌的个体,然后针对性地补充有益菌或其代谢产物,可能实现更精准有效的体重管理。
这种个性化方法的实现需要多方面的技术支撑。首先需要建立标准化的肠道菌群检测和分析流程,能够快速准确地评估个体的微生物组状态。其次需要积累大量的人群数据,建立菌群特征与代谢表型的预测模型。最后需要开发多样化的微生物干预产品,包括不同的益生菌菌株、益生元配方或细菌代谢产物,以满足不同个体的需求。
肥胖是一个多因素疾病,遗传、饮食、运动、睡眠、压力等诸多因素都起作用。肠道菌群干预不太可能成为解决肥胖问题的唯一方案,但它可以成为综合管理策略的重要组成部分。与饮食调整、运动锻炼等生活方式干预相结合,基于微生物组的精准营养和代谢调控可能为肥胖预防和治疗开辟新的途径。克拉格团队的研究为这一愿景提供了坚实的科学基础,也为未来的转化研究指明了方向。